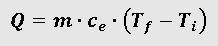La energía el motor de la vida: La Energía Térmica
El calor y temperatura, dos conceptos muy relacionados con la energía térmica, son muy frecuentes en nuestra vida cotidiana. Pero ¿estamos seguros de saber distinguirlos?
A eso nos vamos a dedicar en este tema. Prestaremos atención a:
1. Energía térmica y temperatura
La energía térmica (o energía calorífica) es la que poseen los cuerpos debido al movimiento de las partículasque los forman. Por eso, este movimiento también se llama agitación térmica.
A eso nos vamos a dedicar en este tema. Prestaremos atención a:
- Comprender la diferencia que existe entre el calor y la temperatura (no son la misma cosa)
- Conocer y usar las unidades en las que se suelen medir calor y temperatura.
- Hacer cálculos relacionados con los intercambios de calor entre dos cuerpos y las variaciones de temperatura que producen en ellos.
1. Energía térmica y temperatura
La energía térmica (o energía calorífica) es la que poseen los cuerpos debido al movimiento de las partículasque los forman. Por eso, este movimiento también se llama agitación térmica.
|
La energía térmica que posee un cuerpo no se puede medir y tampoco calcular, puesto que es imposible conocer los detalles del movimiento de cada una de la inmensa cantidad de partículas que forman un cuerpo.
Sin embargo, la agitación térmica de las partículas que forman un cuerpo está relacionada con su temperatura: Cuanta mayor sea la temperatura de un cuerpo, mayor es la agitación térmica y la cantidad de energía térmica que posee. |
2. Calor y temperatura
|
Al poner en contacto dos cuerpos con diferente temperatura, podremos comprobar cómo, al cabo de cierto tiempo (más o menos largo, según el caso) ambos cuerpos terminan por tener la misma temperatura.
En ese momento, los físicos dicen que los cuerpos han alcanzado el equilibrio térmico. Para llegar al equilibrio térmico el cuerpo caliente transfiere calor al más frío. |
IMPORTANTE:
|
3. Unidades de medida
La unidad de calor en el Sistema Internacional, como del resto de las energías, es el julio (J).
Sin embargo, es frecuente que el calor se mida en calorías (cal) o kilocalorías (kcal), como se puede ver en la información nutricional de la etiqueta de los alimentos.
La temperatura es sólo la magnitud que miden los termómetros. Se mide en grados.
4. Calor intercambiado y variación de temperatura
Cuando dos cuerpos se ponen en contacto un tiempo suficiente, terminan por tener la misma temperatura, por alcanzar el equilibrio térmico. Pero ¿de qué dependerá la temperatura final a la que alcancen ese equilibrio térmico?
5. Haciendo cuentas con la temperatura y el intercambio de calor
La unidad de calor en el Sistema Internacional, como del resto de las energías, es el julio (J).
Sin embargo, es frecuente que el calor se mida en calorías (cal) o kilocalorías (kcal), como se puede ver en la información nutricional de la etiqueta de los alimentos.
La temperatura es sólo la magnitud que miden los termómetros. Se mide en grados.
- En nuestra vida cotidiana, usamos el grado centígrado o Celsius (ºC).
- En los países anglosajones emplean el grado Farenheit (ºF).
- En el Sistema Internacional se emplea el kelvin (K).
4. Calor intercambiado y variación de temperatura
Cuando dos cuerpos se ponen en contacto un tiempo suficiente, terminan por tener la misma temperatura, por alcanzar el equilibrio térmico. Pero ¿de qué dependerá la temperatura final a la que alcancen ese equilibrio térmico?
- Cuanto mayor sea la masa de un cuerpo, más calor debe ganar o perder para que su temperatura cambie una cantidad concreta
- La distinta capacidad de los materiales para cambiar de temperatura cuando ganan o pierden calor se llama calor específico. El calor específico de una sustancia nos indica cuánto calor debe ganar o perder 1 kg de una sustancia para que su temperatura varíe 1 K (o 1 ºC).
5. Haciendo cuentas con la temperatura y el intercambio de calor
|
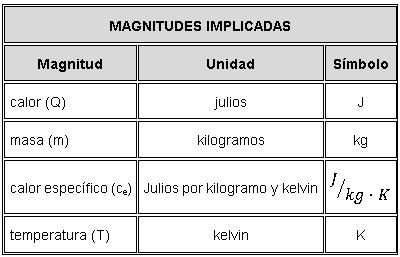
Lo primero que tienes que tener claro antes de nada es la fórmula que vamos a usar para hacer los cálculos, las magnitudes implicadas en la misma y sus unidades en el Sistema Internacional.
Pero no te asustes que no es tan complicado como parece:
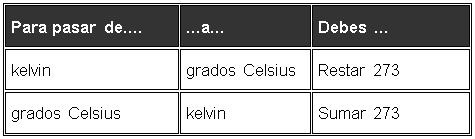
Recuerda que a la hora de hacer cuentas es fundamental que todas las magnitudes estén en las unidades del SI. Por eso, a veces tendrás que pasar de grados Celsius a kelvin o viceversa. La siguiente tabla te recuerda cómo hacerlo: |
Unidades de Medida
|
Ejemplo:
Un trozo de hierro de 200 gramos de masa que se encuentra a 30 ºC, se calienta hasta alcanzar 80 ºC ¿Qué cantidad de calor ha absorbido o desprendido?
Lo primero que tenemos que hacer es convertir todos los datos a las unidades al S.I. En este caso convertiremos los gramos en kg, y los ºC en K:
200 g = 0,2 kg 30 ºC = 303 ºK 80 ºC = 353 K
Tenemos que buscar en la tabla de calores específicos el que corresponda al hierro, material con el que estamos trabajando en el problema: ce = 450 J/kg∙K
A continuación sustituimos en la fórmula los valores de las magnitudes conocidas; todas en este caso, excepto el calor, que es precisamente lo que queremos calcular:
Q = 0,2 kg ∙ 450 J/kg∙K ∙ (353 K - 303 K)
Ahora hacemos los cálculos, empezando por el paréntesis:
Q = 0,2 kg ∙ 450 J/kg∙K ∙ 50 K
Q = 4500 J
Solución: El trozo de hierro ha absorbido 4500 J.
El valor obtenido es positivo, lo que significa que el hierro no ha cedido calor, sino que lo ha ganado.
Un trozo de hierro de 200 gramos de masa que se encuentra a 30 ºC, se calienta hasta alcanzar 80 ºC ¿Qué cantidad de calor ha absorbido o desprendido?
Lo primero que tenemos que hacer es convertir todos los datos a las unidades al S.I. En este caso convertiremos los gramos en kg, y los ºC en K:
200 g = 0,2 kg 30 ºC = 303 ºK 80 ºC = 353 K
Tenemos que buscar en la tabla de calores específicos el que corresponda al hierro, material con el que estamos trabajando en el problema: ce = 450 J/kg∙K
A continuación sustituimos en la fórmula los valores de las magnitudes conocidas; todas en este caso, excepto el calor, que es precisamente lo que queremos calcular:
Q = 0,2 kg ∙ 450 J/kg∙K ∙ (353 K - 303 K)
Ahora hacemos los cálculos, empezando por el paréntesis:
Q = 0,2 kg ∙ 450 J/kg∙K ∙ 50 K
Q = 4500 J
Solución: El trozo de hierro ha absorbido 4500 J.
El valor obtenido es positivo, lo que significa que el hierro no ha cedido calor, sino que lo ha ganado.