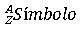Tema 2: La materia: ¿Cómo aparece la materia en la naturaleza?
Coge un trozo de materia, un papel por ejemplo, y divídelo en trozos, ¿será esa la estructura básica de la materia?, sabes que no, porque aún pueden dividirse esos trozos. Divide los trozos en otros menores, y ves que aún podrías seguir dividiéndolos…. Todo esto puede llevar a pensar que en algún momento tras muchos cortes encontrarás el “trozo que no se puede dividir”, el componente básico del papel… los átomos.
Pero… ¿qué es un átomo?
1.- Los átomos
Pero… ¿qué es un átomo?
1.- Los átomos
|
Los átomos son los componentes básicos de la materia. Un átomo está constituido por:
|
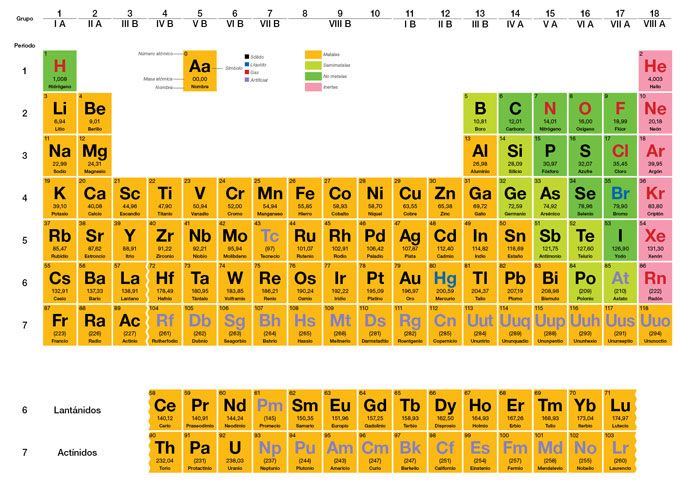
Junto al símbolo, en cada casilla de la tabla periódica aparece un numerito. Pues bien, ese numerito se llama número atómico y nos dice el número de protones que todos los átomos de ese tipo tienen en su núcleo. Se representa por la letra Z.
El número de neutrones se representa con la letra N.
Al número conjunto de protones y neutrones de un átomo (a la suma de los dos) se le llama número másico y se representa por la letra A.
El número de neutrones se representa con la letra N.
Al número conjunto de protones y neutrones de un átomo (a la suma de los dos) se le llama número másico y se representa por la letra A.
Normalmente los átomos son neutros, tienen el mismo número de cargas eléctricas positivas que negativas, es decir, tienen el mismo número de electrones que de protones. Pero puede darse el caso que dos átomos del mismo tipo, con el mismo número de protones, no que tengan distinto número de neutrones, se dice que son isótopos.
En la naturaleza hay 92 tipos de átomos diferentes (y otros cuantos más obtenidos de forma artificial). Cada uno de ellos tiene su nombre y, además, para representarlo de forma sencilla los científicos le han puesto un símbolo con una letra.
En la naturaleza hay 92 tipos de átomos diferentes (y otros cuantos más obtenidos de forma artificial). Cada uno de ellos tiene su nombre y, además, para representarlo de forma sencilla los científicos le han puesto un símbolo con una letra.
2.- Las moléculas
Los átomos no suelen encontrarse libres en la naturaleza; no suelen estar solos, sino en compañía de otros átomos, formando moléculas.
Los átomos no suelen encontrarse libres en la naturaleza; no suelen estar solos, sino en compañía de otros átomos, formando moléculas.
Una molécula es una combinación de dos o más átomos que se mantienen fuertemente unidos.
Todas las moléculas de una determinada sustancia son exactamente iguales, y diferentes a las de todas las demás sustancias.
3.- ¿Son capaces de organizarse las partículas para formar la materia?
La explicación que buscamos nos la da la teoría cinético molecular, una teoría muy sencilla que se puede resumir en las siguientes ideas:
La explicación que buscamos nos la da la teoría cinético molecular, una teoría muy sencilla que se puede resumir en las siguientes ideas:
- La materia está constituida por partículas independientes, separadas entre sí, ya sean átomos o moléculas.
- Las partículas tienen masa y se atraen entre sí, (fuerzas de cohesión), tanto mas más cuanto más cerca estén, pero si se acercan demasiado, empiezan a repelerse...
- Entre las partículas no hay nada, sólo espacio vacío, que es mayor en gases que en líquidos y, en éstos, mayor que en sólidos.
- Las partículas se mueven constantemente en línea recta y en todas direcciones: en gases lo hacen libremente, en líquidos con menos libertad y en sólidos vibran en torno a posiciones fijas.
- A mayor temperatura, más rápido es el movimiento de las partículas y, por tanto, mayor es su energía cinética.
4.- Los tres estados de la materia
Que una sustancia esté en un estado u otro depende de cómo estén unidas entre si las moléculas que lo forman, es decir, de cómo sea el equilibrio entre las fuerzas de atracción y repulsión entre las moléculas y de lo rápido que se estén moviendo.
Por lo que podemos decir que:
Que una sustancia esté en un estado u otro depende de cómo estén unidas entre si las moléculas que lo forman, es decir, de cómo sea el equilibrio entre las fuerzas de atracción y repulsión entre las moléculas y de lo rápido que se estén moviendo.
- Lo primero depende del tipo de moléculas de las que esté hecho el cuerpo, es decir, de la sustancia concreta de que se trate.
- Lo segundo depende de la temperatura a la que esté el cuerpo.
Por lo que podemos decir que:
- En los gases apenas hay fuerzas entre las moléculas y por eso éstas se mueven libremente.
- En los líquidos las fuerzas entre las moléculas son más intensas que en los gases. Por eso se mantienen unidas, pero aún conservan gran libertad de movimiento (aunque menos que en los gases)
- En los sólidos las fuerzas entre las moléculas son muy intensas. Tanto que prácticamente no pueden moverse, tan solo vibrar.
4.1.- Los gases
En un gas las fuerzas entre las partículas son escasas, tanto que podemos considerarlas como "cuerpos libres", sin interacción alguna como se ven en la animación.
De aquí se derivan las propiedades más importantes de los gases:
4.2.- Los líquidos
La diferencia de los líquidos con los gases, es que sí existen fuerzas entre las moléculas. Cada molécula interacciona con sus vecinas, lo bastante fuerte como para no poder separarse de ellas, pero no tanto como para impedir que puedan desplazarse unas respecto a otras.
Ahora ya no hay grandes espacios entre las moléculas; están casi juntas, pero no fijas en un sitio. Ese comportamiento de las moléculas se traduce en las propiedades que vemos de los líquidos:
4.3.- Los sólidos
En el caso de los sólidos, se siguen moviendo, como en líquidos y gases, pero ahora tienen muy poca libertad de movimiento, solo pueden vibrar alrededor de sus posiciones de equilibrio.
Este comportamiento de las moléculas de un sólido se traduce en las propiedades que observamos de ellos:
En un gas las fuerzas entre las partículas son escasas, tanto que podemos considerarlas como "cuerpos libres", sin interacción alguna como se ven en la animación.
De aquí se derivan las propiedades más importantes de los gases:
- Los gases no tienen forma ni volumen propio, adoptan la forma y el volumen del recipiente que los contiene.
- Los gases pueden comprimirse y expandirse.
- Los gases ejercen presión (empujan) sobre cualquier superficie que tocan, en todas direcciones (incluso hacia arriba)
4.2.- Los líquidos
La diferencia de los líquidos con los gases, es que sí existen fuerzas entre las moléculas. Cada molécula interacciona con sus vecinas, lo bastante fuerte como para no poder separarse de ellas, pero no tanto como para impedir que puedan desplazarse unas respecto a otras.
Ahora ya no hay grandes espacios entre las moléculas; están casi juntas, pero no fijas en un sitio. Ese comportamiento de las moléculas se traduce en las propiedades que vemos de los líquidos:
- Los líquidos no tienen forma propia, pero sí volumen propio.
- Los líquidos no pueden ni comprimirse ni expandirse.
- Los líquidos son fluidos, pueden derramarse.
4.3.- Los sólidos
En el caso de los sólidos, se siguen moviendo, como en líquidos y gases, pero ahora tienen muy poca libertad de movimiento, solo pueden vibrar alrededor de sus posiciones de equilibrio.
Este comportamiento de las moléculas de un sólido se traduce en las propiedades que observamos de ellos:
- Los sólidos tienen forma y volumen fijos.
- Los sólidos no pueden ni comprimirse ni expandirse.
- Los sólidos no fluyen, no se derraman.
5.- Los cambios de estado
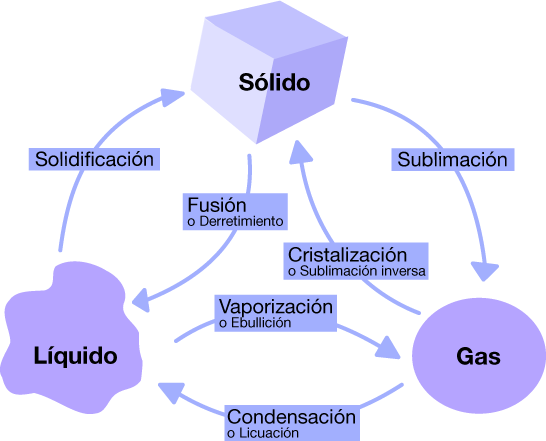
Observa cómo se llaman todos los cambios de estado que pueden producirse:
Observa cómo se llaman todos los cambios de estado que pueden producirse:
Cualquier sustancia puede estar en cualquiera de los tres estados de agregación; todo depende de la temperatura a la que se encuentre y a las característicos de cada sustancia.